引言
GMP洁净室设计规范是针对制药、生物制品等行业生产环境的规范要求,旨在确保生产过程的安全性、有效性和产品质量。GMP(Good Manufacturing Practice)即良好生产规范,是一套确保产品生产、加工、包装和储存符合特定标准和要求的体系。本文将详细介绍GMP洁净室的设计规范,包括设计原则、分类、设施要求以及维护管理等。
设计原则
GMP洁净室的设计应遵循以下原则:
安全性:确保生产过程中人员和产品的安全,防止交叉污染。
可靠性:保证洁净室的运行稳定,减少故障和停机时间。
易于清洁:便于清洁和消毒,减少细菌和病毒的滋生。
经济性:在满足规范要求的前提下,尽量降低建设和运营成本。
洁净室分类
根据洁净度要求,GMP洁净室可分为以下几类:
A级洁净室:适用于无菌药品的生产,如注射剂、细胞治疗制品等。
B级洁净室:适用于高风险药品的生产,如眼药水、耳鼻喉科用药等。
C级洁净室:适用于中风险药品的生产,如口服固体、外用药等。
D级洁净室:适用于低风险药品的生产,如原料药、中间体等。
洁净室的分类标准依据《药品生产质量管理规范》(GMP)和相关国际标准。
设施要求
GMP洁净室的设计应满足以下设施要求:
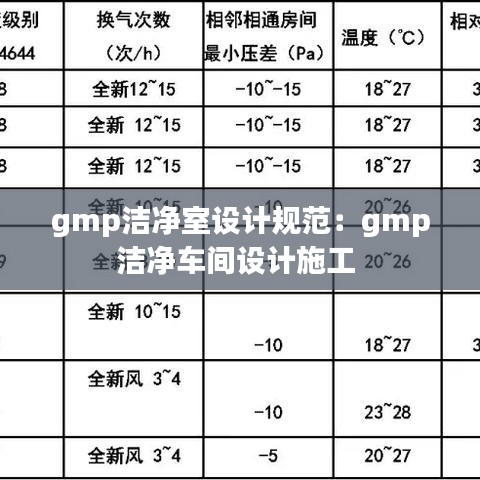
空气处理系统:包括空气过滤、加湿、除湿、温度控制等,确保室内空气质量符合要求。
送风和排风系统:合理布局,确保洁净空气的供应和污染物的排出。
压差控制:通过正压或负压控制,防止污染空气进入洁净室。
地面和墙面:采用易于清洁、消毒的材料,如防滑瓷砖、不锈钢等。
门窗:密封性能良好,防止外界污染进入。
照明:采用无影灯,避免对产品质量造成影响。
清洁工具和设备:专用清洁工具,避免交叉污染。
维护管理
GMP洁净室在使用过程中,应加强维护管理,确保其持续符合规范要求:
定期检测:对洁净室的空气、尘埃、微生物等进行定期检测,确保其符合规范要求。
清洁消毒:定期进行清洁和消毒,防止污染。
设备维护:定期对设备进行检查、保养和维修,确保其正常运行。
人员培训:对操作人员进行GMP规范和洁净室操作培训,提高其专业技能。
总结
GMP洁净室设计规范是制药、生物制品等行业生产环境的重要组成部分,对于确保产品质量和人员安全具有重要意义。在设计、建设和使用过程中,应严格按照规范要求进行,确保洁净室的有效性和可靠性。同时,加强维护管理,确保洁净室始终处于良好状态,为我国制药行业的健康发展提供有力保障。
转载请注明来自互诺实验设备(衡水)有限公司,本文标题:《gmp洁净室设计规范:gmp洁净车间设计施工 》










 冀ICP备2024085275号-1
冀ICP备2024085275号-1
还没有评论,来说两句吧...